Respinsă cererea farmaciilor de a continua producția medicamentelor
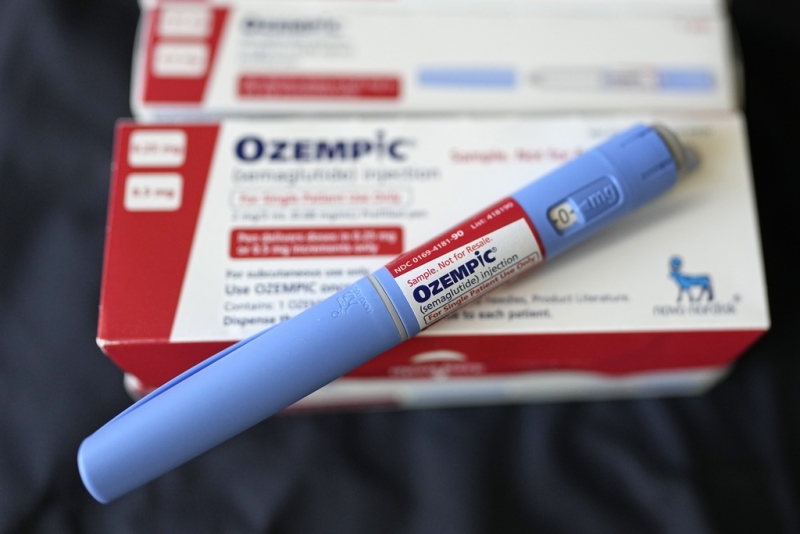
Un judecător din Statele Unite a refuzat, joi, solicitarea farmaciilor de a continua fabricarea copiilor medicamentelor Ozempic și Wegovy, cele destinate tratamentului diabetului și pierderii în greutate, produse de compania Novo Nordisk. Decizia a fost comunicată prin documentele judiciare, conform informațiilor provenite de la mediafax. Această hotărâre a fost luată în urma unei acțiuni legale inițiate în luna februarie de un grup din industria farmaceutică de compounding, contestând decizia Administrației americane pentru alimente și medicamente (FDA), care a afirmat că nu mai există o penurie a ingredientului activ al acestor medicamente, semaglutida.
Contextul contestației legale
Cererea inițială din partea celor care activează în domeniul compounding a fost de a continua producția medicamentelor de acest tip, având în vedere cererea crescută pe piață. Industria de compounding combină, amestecă și modifică ingredientele medicamentelor de marcă care sunt în criză, pentru a răspunde nevoilor pacienților. În trecut, aceste farmacii au fost autorizate să producă zeci de mii de doze de copii ale medicamentelor Novo destinate tratamentului obezității și diabetului, numai în perioada în care FDA a declarat o penurie. Multe dintre aceste produse sunt comercializate de companii mari de telemedicină, cum ar fi Hims & Hers.
Decizia judecătorului Mark Pittman
Judecătorul federal Mark Pittman din Texas a emis o hotărâre prin care a respins cererea farmaciilor de a obține o interdicție preliminară. Deși argumentele sale juridice au fost prezentate sub sigiliu, respingerea cererii de interdicție înseamnă că termenul stabilit de FDA pentru încetarea activității companiilor de compounding rămâne activ. Această hotărâre urmează unei decizii anterioare a judecătorului, care a refuzat permisiunea farmaciilor de a produce copii ale altor medicamente pentru pierderea în greutate și diabet, cum ar fi Zepbound și Mounjaro, fabricate de Eli Lilly.
Reacția companiilor și organizațiilor
Reprezentanții FDA și Novo Nordisk nu au oferit imediat comentarii legate de această decizie. Într-o declarație anterioară, Novo Nordisk a susținut că FDA a ajuns la concluzia că producția de medicamente de către companie a depășit orice estimare rezonabilă a cererii de pe piață. Această declarație subliniază încrederea companiei în evaluările agenției de reglementare, în contextul crizei de medicamente.
Dovezi de penurie prezentate de Outsourcing Facilities Association
Lee Rosebush, președintele Outsourcing Facilities Association, principalul reclamant în acest proces, a declarat pentru Reuters că organizația sa a adus dovezi care indică o continuare a penuriei de semaglutid, descoperită după intentarea procesului. Cu toate acestea, Rosebush a remarcat că judecătorul a ales să nu ia în considerare aceste dovezi în decizia sa. „Suntem evident dezamăgiți de această hotărâre inițială și credem că datele sugerează că există în continuare o penurie a acestor produse,” a adăugat el.
Impactul asupra pacienților și industriei farmaceutice
Refuzul judecătorului de a permite continuarea producerii medicamentelor de către farmacii poate avea un impact semnificativ asupra pacienților care depind de aceste tratamente. De asemenea, poate afecta și sectoarele compounding, care au investit resurse considerabile în producerea acestor medicamente. Decizia subliniază tensiunile existente între reglementările FDA și nevoile pacienților, într-o perioadă în care crizele de medicamente devin tot mai frecvente.
Experiențele pacientului și alternativa de tratament
Pentru pacienți, gestionarea diabetului și obezității este deja o provocare, iar lipsa accesului la medicamentele necesare poate agrava problemele de sănătate. În acest context, pacienții ar putea fi nevoiți să caute alternative de tratament sau să se bazeze pe medicamente care nu răspund pe deplin nevoilor lor. Această situație evidențiază importanța unei reglementări eficiente care să echilibreze nevoile pacienților, siguranța produselor și viabilitatea industriilor farmaceutice.
Punctul de vedere al experților
Experții subliniază faptul că, în timp ce responsabilitatea FDA este de a asigura că medicamentele sunt sigure și că oferta corespunde cererii, este crucial să se asigure și accesibilitatea medicamentelor esențiale. Prin urmare, deciziile luate în privința compounding-ului acestor medicamente trebuie să țină cont atât de cerințele legale, cât și de bunăstarea pacienților.
Consecințe pe termen lung pentru industrie
Decizia judecătorului de a menține restricțiile asupra producției medicamentelor de către farmacii ar putea determina o reevaluare a strategiilor din cadrul industriei de compounding. Este esențial ca aceste firme să se adapteze noilor condiții și să găsească modalități de a oferi soluții inovatoare, continuând să colaboreze cu autoritățile de reglementare pentru a asigura accesul la produse farmaceutice în condiții de maximală siguranță.